Синтез и особенности структуры комплексных соединений La(III) с органическими лигандами
Синтез и особенности структуры комплексных соединений La(III) с органическими лигандами
Аннотация
В работе осуществлено получение и исследование физико-химических характеристик азотсодержащих комплексных соединений лантана с никотиновой кислотой, никотиновой кислотой и гексаизотиоцианохроматом (III) калия, уротропином и метаванадиевой кислотой, и спирокарбоном (4,4,10,10-тетраметил-1,3,7,9-тетраазоспиро[5,5]ундекан 2,8-дионом). Проведён большой синтетический эксперимент, направленный на смещение равновесия реакций комплексообразования в сторону продуктов, подбор правильной последовательности добавления реагентов и условий химических превращений, а также выделение чистых комплексных соединений из реакционной массы от примесей. Для комплексов состава [La(C6H5COO)3] и La(VO3)3·8HVO3·2Hexa·4H2O (где Hexa – уротропин) были применены усовершенствованные методики получения.
1. Введение
Лантан не входит в число эссенциальных химических элементов , обнаружен в небольших количествах в организме человека, но способен существенно влиять на биологические процессы . В медицине соединения лантаноидов применяются при диагностике и лечении заболеваний (в том числе и онкологических) , достижения в области нанотехнологий дают возможность доставки лекарств . Никотиновая кислота, будучи составной частью комплексных соединений, облегчает усвоение ионов d-металлов (хрома, цинка и др.) , а также участвует в синтезе и расщеплении жирных кислот и углеводов . Уротропин также является дешёвым и перспективным лигандом . Атомы азота, присутствующие в данном лиганде, могут функционировать как дополнительные центры адсорбции или каталитически активные центры .
Целью работы является синтез и исследование физико-химических, характеристик азотсодержащих комплексных соединений лантана с никотиновой кислотой, никотиновой кислотой и гексаизотиоцианохроматом (III) калия, уротропином и метаванадиевой кислотой, и спирокарбоном (4,4,10,10-тетраметил-1,3,7,9-тетраазоспиро[5,5]ундекан2,8-дионом).
ИК-спектры были получены на спектрометре “Spectrum 65”. Электронные спектры поглощения регистрировались с помощью спектрофотометра “ПЭ-5400УФ” производителя Экросхим.
2. Экспериментальная часть
Комплекс лантана с никотиновой кислотой состава [La(C4H5NCOOH)3] был получен двумя способами. Первый включает в себя прямое взаимодействие между раствором с ионами La3+ и трёхкратным избытком лиганда при рН=4, после чего прозрачный раствор медленно упаривают. Наблюдалось выпадение белого, трудно растворимого в воде осадка. Комплекс хорошо растворим в этаноле и изопропаноле. Второй способ можно представить схемой, представленной ниже. Важно упомянуть, что реакция 2 проводится в слабокислой среде во избежание выпадения La(OH)3.
1) C5H4NCOOH + NaOH → C5H4NCOONa + H2O;
2) 3C5H4NCOONa + La(NO3)3·6H2O → [La(C4H5NCOO)3]↓ + 3NaNO3 + 6H2O.
Структура полученного комплекса изображена на рис. 1.
![Структура комплекса [La(C6H5COO)3]](/media/images/2024-03-14/ed149aeb-b610-4785-b909-16640d1fd56c.png)
Рисунок 1 - Структура комплекса [La(C6H5COO)3]
Гекса(изотиоцианато)хромат(III) лантана был получен смешиванием K3[Cr(NCS)6]∙H2O (10 ммоль вещества в водном растворе) и никотиновой кислоты (30 ммоль) с последующим добавлением 4,33 г La(NO3)3∙6H2О при рН=4-6. При охлаждении в течение 30 минут наблюдалось выпадение бледно-сиреневого осадка. Неорганическое координационное соединение образовалось при смешении солей согласно реакции: 6KSCN + CrCl3 → K3[Cr(NCS)6] + 3KCl.
Постепенно цвет раствора менялся с ярко-зелёного до тёмно-фиолетового, почти переходящего в чёрный. Структура комплекса отображена на рис. 2.
![Структура комплекса [La(C4H5NCOOH)3(H2O)2][Cr(NCS)6]](/media/images/2024-03-14/003db7da-7edf-4983-8478-6bd6fb66bc0c.png)
Рисунок 2 - Структура комплекса [La(C4H5NCOOH)3(H2O)2][Cr(NCS)6]
Двойные комплексные соли подобного состава широко применяются на практике в качестве прекурсоров для нанокомпозитов и функциональных материалов .
Координационное соединение со спирокарбоном, обладающее структурой {[LaSk2(H2O)(NO3)2](NO3)}, где Sk – спирокарбон , было получено реакцией между навеской 4,33 г La(NO3)3∙6H2О, растворённой в ацетоне, и последующим добавлением к ней 2,41 г белого порошка лиганда. Вязкий раствор был отфильтрован, фильтрат хранился в холодильнике в плотно закупоренном сосуде. Примерно через месяц сформировались легко растворимые в воде прозрачные кристаллы. Строение комплекса изображено на рисунке 3.
}](/media/images/2024-03-14/25386384-3458-4d99-ada1-05ee0e3ada78.png)
Рисунок 3 - Структура комплекса {[LaSk2(H2O)(NO3)2](NO3)}
1) 2NH4VO3 → V2O5 + 2NH3 + H2O – при нагревании;
2) V2O5 + H2O → 2HVO3 – при нагревании;
3) 11HVO3 + La(NO3)3∙6H2О + 2Hexa → La(VO3)3∙8HVO3∙2Hexa∙4H2O.
Бурый с фиолетовым оттенком порошок растворяется при нагревании в воде (реакция 2), после чего раствор почти мгновенно приобретает лимонно-жёлтую окраску. Остаток непрореагировавшего оксида отфильтровывался под вакуумом; для дальнейших манипуляций необходим прозрачный раствор. Реакция 3 должна проходить при рН в интервале от 3 до 5; использование буферного раствора при проведении эксперимента не требовалось. Данные о структуре полученного соединения представлены на рисунке 4.
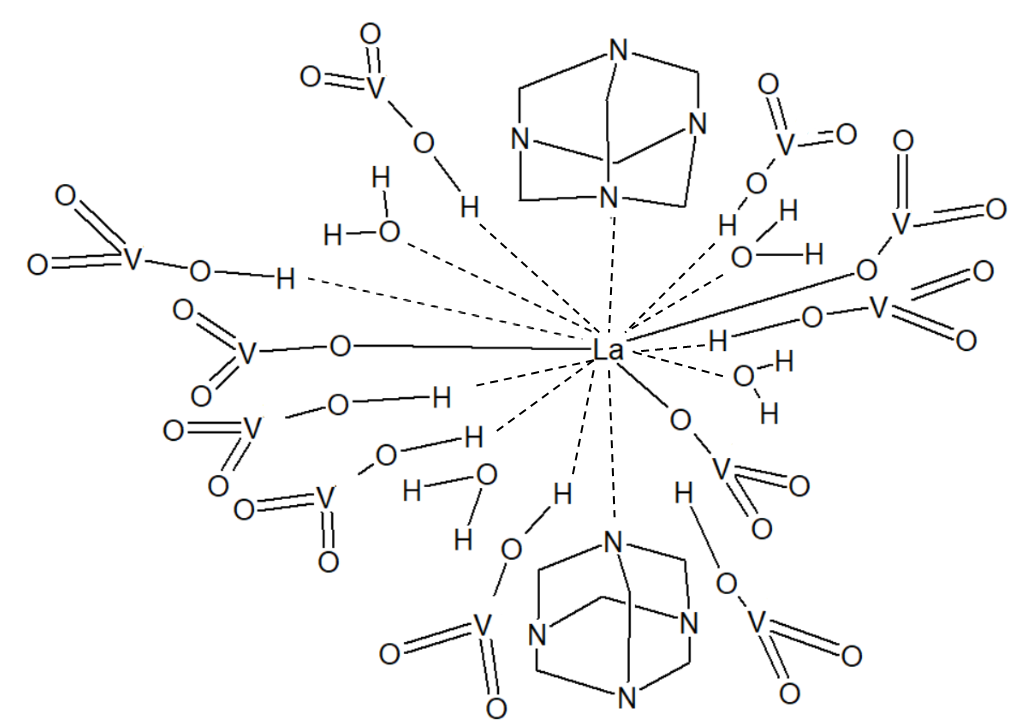
Рисунок 4 - Структура комплекса La(VO3)3·8HVO3·2Hexa·4H2O
3. Обсуждение
Анализ ИК-спектров исследуемых соединений показал сдвиг колебательных частот в область более коротких волн. У никотината лантана пик C=O сместился с 1714,62 см-1 у лиганда (см. рис. 5) до 1546,81 см-1 (см. ИК спектр на рис. 6), что подтверждает образование соли.
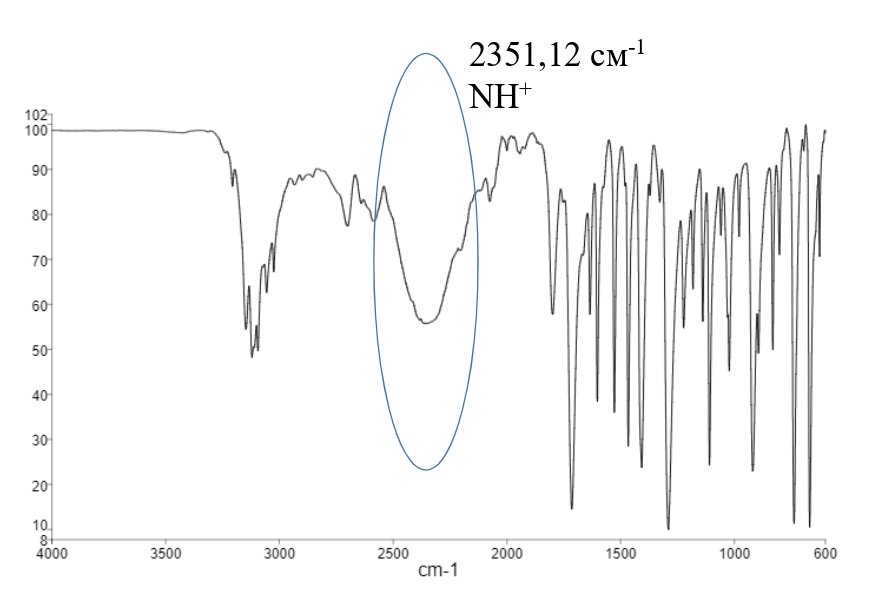
Рисунок 5 - ИК-спектр никотиновой кислоты
![ИК-спектр комплекса [La(C6H5COO)3]](/media/images/2024-03-14/176271a9-2802-4adc-8b9b-6a422ec7b417.png)
Рисунок 6 - ИК-спектр комплекса [La(C6H5COO)3]
У [La(C4H5NCOOH)3(H2O)2][Cr(NCS)6] волновое число группировки NCS с 2057,43 см-1 (см. ИК спектр лиганда на рис. 7) меняется до значения 2053,57 см-1 (см. рис. 8); это доказывает у изотиоцианат-аниона участие в формировании второй внутренней сферы комплекса.
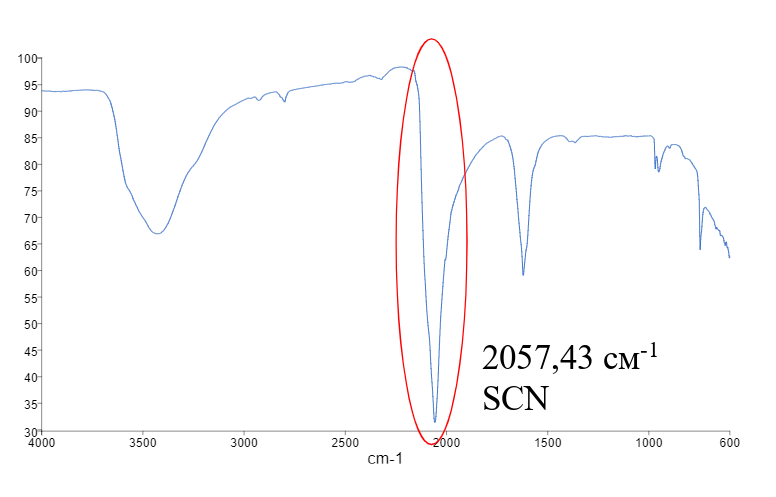
Рисунок 7 - ИК-спектр гексаизотиоцианохромата (III) калия
![ИК-спектр комплекса [La(C4H5NCOOH)3(H2O)2][Cr(NCS)6]](/media/images/2024-03-14/0e283087-3c03-42de-944c-c3373cef8a04.png)
Рисунок 8 - ИК-спектр комплекса [La(C4H5NCOOH)3(H2O)2][Cr(NCS)6]
У никотинатов отсутствует пик от протонированной формы никотиновой кислоты в 2351,12 см-1, что говорит о построении получившихся координационных соединений через азот. Через кислород связывается катион лантана в комплексе со спирокарбоном – волновое число С=О изменяется с 1650,67 см-1 (см. ИК спектр лиганда на рис. 9) до 1636,99 см-1 (см. ИК спектр образовавшегося соединения на рис. 10).
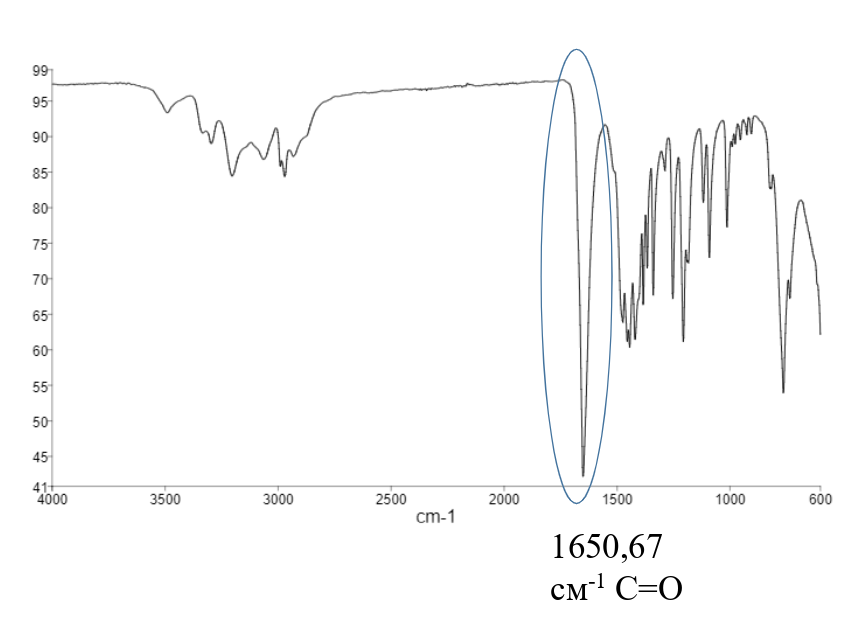
Рисунок 9 - ИК-спектр спирокарбона
}](/media/images/2024-03-14/d03fa9cc-5366-4aa6-a46d-1ed75130140f.png)
Рисунок 10 - ИК-спектр комплекса {[LaSk2(H2O)(NO3)2](NO3)}
У комплекса La(VO3)3∙8HVO3∙2Hexa∙4H2O меняются волновые числа: соответствующие C-N от уротропина с 1238,43 см-1 (см. рис. 11) до 1234,49 см-1 (см. рис. 13), а также от метаванадиевой кислоты с 1398,52 см-1 до 1379,87 см-1(см. рис. 12 и рис.13 соответственно).
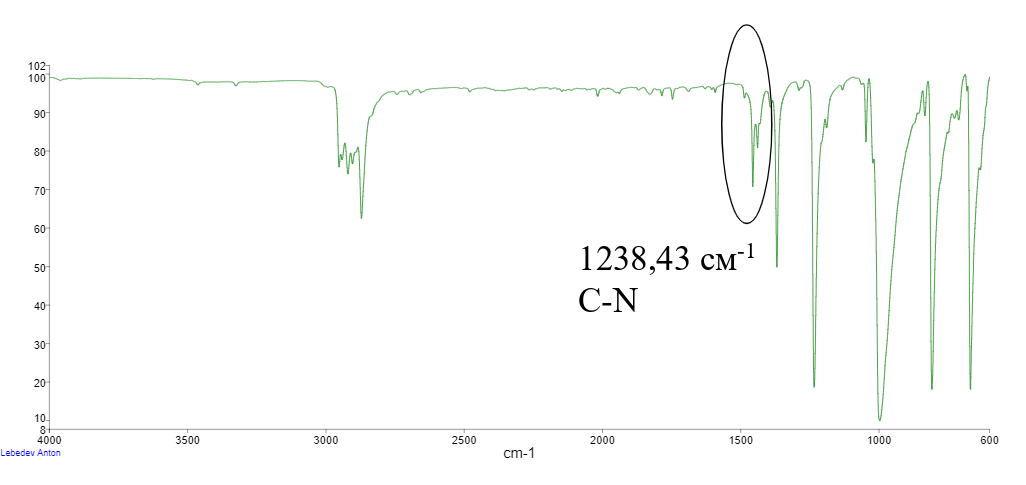
Рисунок 11 - ИК-спектр уротропина
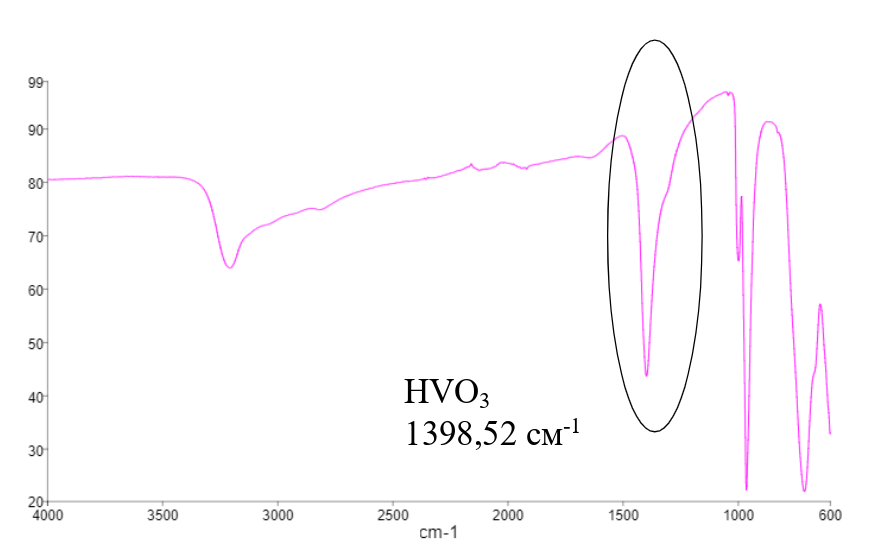
Рисунок 12 - ИК-спектр HVO3
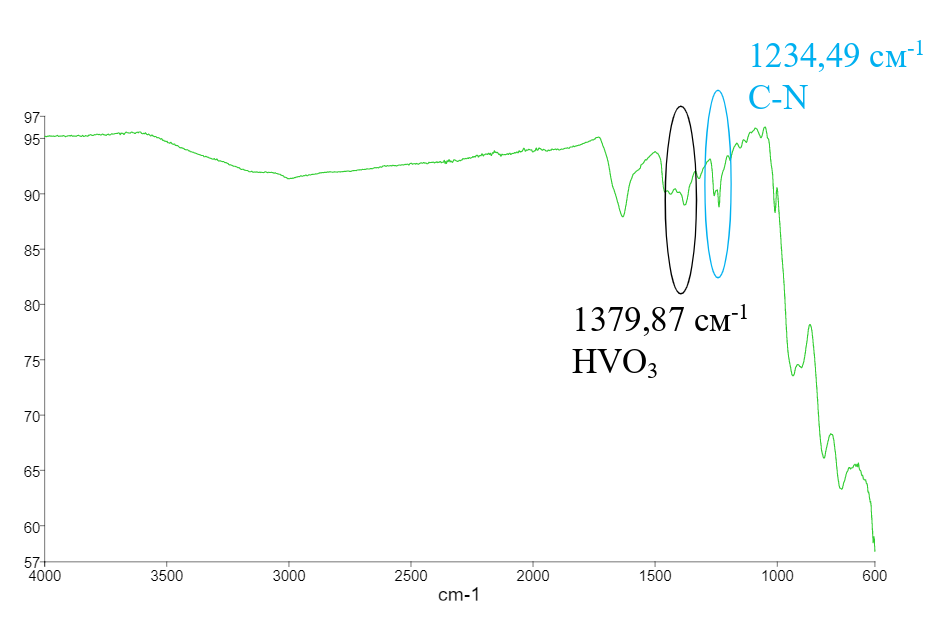
Рисунок 13 - ИК-спектр комплекса La(VO3)3·8HVO3·2Hexa·4H2O
Электронная структура полученных комплексных соединений лантана менялась относительно их лигандов. Например, при сравнении электронных спектров поглощения K3[Cr(SCN)6], λmax которого составляет 211 нм, а также никотиновой кислоты с пиком максимума в 243 нм, наблюдалось смещение максимума поглощения до величины 315 нм (см. рис. 14). Это может свидетельствовать о высокой степени комплексообразования перечисленных соединений с ионом La3+.
![Рисунок 14 - УФ спектр [La(C4H5NCOOH)3(H2O)2][Cr(NCS)6] (серая линия), никотиновой кислоты (оранжевая линия), гексаизотиоцианохромата (III) калия (синяя линия)](/media/images/2024-03-14/3d4c62ca-633e-4817-aea6-3aa4390dd071.png)
Рисунок 14 - Рисунок 14 - УФ спектр [La(C4H5NCOOH)3(H2O)2][Cr(NCS)6] (серая линия), никотиновой кислоты (оранжевая линия), гексаизотиоцианохромата (III) калия (синяя линия)
Образование комплексов лантана с органическими лигандами для электронных спектров каждого из образцов можно подтвердить наличием следующих батохромных сдвигов (см. табл.1):
Таблица 1 - Значения λmax в электронных спектрах лигандов и комплексных соединений
№ | λmax лиганда, нм | λmax комплекса, нм |
[La(C6H5COO)3] | 243 (никотиновая кислота) | 261 |
[La(C4H5NCOOH)3(H2O)2][Cr(NCS)6] | 243 - никотиновая кислота; 211 - K3[Cr(SCN)6]. | 315 |
{[LaSk2(H2O)(NO3)2](NO3)} | 209 – спирокарбон | 241 |
La(VO3)3·8HVO3·2Hexa·4H2O | 189 – уротропин | 255 |
4. Определение констант нестойкости
Константы нестойкости полученных соединений определяли спектрофотометрическим методом. Для этого была приготовлена серия из 7 стандартных растворов комплексов. Необходимо, чтобы выбранный интервал концентраций соответствовал области возможных изменений концентраций анализируемого раствора. По мере роста концентрации наблюдался рост абсорбции, прекращение которого наступало по мере насыщаемости раствора (см. табл. 2). Концентрация, при которой значение абсорбции впоследствии стало неизменным или изменялось незначительно, принималось за растворимость s комплексного соединения. Исходя из данных о растворимости, рассчитывались константы нестойкости комплексных соединений, отрицательный десятичный логарифм которых приведён в таблице 3.
Были построены графики зависимости абсорбции от концентрации для каждого из комплексов (см. рис. 15, 16, 17, 18).
![график насыщаемости комплекса [La(C4H5NCOOH)3]](/media/images/2024-03-14/4f4ac6b7-0513-42c6-8208-5372c98d083b.png)
Рисунок 15 - график насыщаемости комплекса [La(C4H5NCOOH)3]
![график насыщаемости комплекса [La(C4H5NCOOH)3][Cr(NCS)6]](/media/images/2024-03-14/d05aa947-8557-4b6b-a8e8-ea0283814eaa.png)
Рисунок 16 - график насыщаемости комплекса [La(C4H5NCOOH)3][Cr(NCS)6]
![График насыщаемости комплекса {LaSk2(H2O)(NO3)2]{(NO3)}](/media/images/2024-03-14/55234a52-31ab-48b4-85fb-75d50984213f.png)
Рисунок 17 - График насыщаемости комплекса {LaSk2(H2O)(NO3)2]{(NO3)}
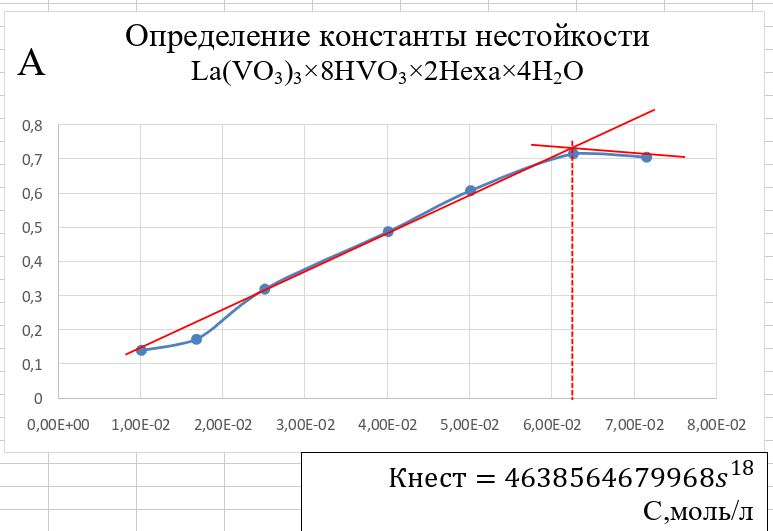
Рисунок 18 - График насыщаемости комплекса La(VO3)3·8HVO3·2Hexa·4H2O
В качестве примера можно привести график насыщаемости с таблицы 3, построенный для определения константы нестойкости никотината лантана (см. рис. 15).
Таблица 2 - Значения абсорбции, соответствующие концентрации растворов никотината лантана
C, моль/л | А |
1,00·10-4 | 0,241 |
6,25·10-4 | 0,357 |
1,00·10-3 | 0,406 |
2,50·10-3 | 0,552 |
8,33·10-3 | 0,733 |
1,00·10-2 | 0,776 |
1,25·10-2 | 0,769 |
5. Заключение
Были подобраны оптимальные условия и выполнены синтезы азотсодержащих комплексных соединений лантана со следующими лигандами: никотиновой кислотой, никотиновой кислотой и гексаизотиоцианатохромат (III)-анионом, уротропином и спирокарбоном. Для комплексов состава [La(C6H5COO)3] и La(VO3)3·8HVO3·2Hexa·4H2O (где Hexa – уротропин) были применены усовершенствованные методики получения Аналитические сигналы, подтверждающие изменения в структуре – максимумы поглощения при следующих длинах волн: λmax1=261 нм, λmax2=315 нм, λmax3=241 нм, λmax4=255 нм. Спектрофотометрическим методом были определены константы нестойкости, отрицательные десятичные логарифмы значений которых приведены в таблицe 3.
Таблица 3 - Значения десятичных логарифмов констант нестойкости комплексов
Комплекс | lg β |
{[LaSk2(H2O)(NO3)2](NO3)} | 4,79 |
[La(C6H5COO)3] | 6,57 |
La(VO3)3×8HVO3×2Hexa×4H2O | 10,00 |
[La(C4H5NCOOH)3(H2O)2][Cr(NCS)6] | 19,02 |
