Homologous series of chemical compounds of the system (Ca2+ – Ir4+ – Ir5+ – O2-) based on the compound Ca10Ir4+5Ir5+4O30
Homologous series of chemical compounds of the system (Ca2+ – Ir4+ – Ir5+ – O2-) based on the compound Ca10Ir4+5Ir5+4O30
Abstract
The paper presents for the first time the calculation of formulas for homologous series of chemical compounds of a four-component system (Ca2+ – Ir4+ – Ir5+ – O2-) based on the compound Ca10Ir4+5Ir5+4O30. The formulas Ca20n -10Ir4+5Ir5+4O20n + 10, Ca10Ir4+10n - 5Ir5+4O20n + 10 and Ca10Ir4+5Ir5+8n - 4O20n + 10 reflect the development of homologous series towards CaO, IrO2 and Ir2O5. Three-component compounds Ir4+5Ir5+4O20, Ca2Ir4+O4, and Ca5Ir5+2O10 were used in the calculation, which were the first basic compounds in a chain of sequential chemical interactions in three component subsystems (Ir4+ – Ir5+ – O2-), (Ca2+ – Ir4+ – O2-) and (Ca2+ – Ir5+ – O2-) starting with the formation of CaO, IrO2 and Ir2O5. Compounds Ir4+5Ir5+4O20, Ca2Ir4+O4, and Ca5Ir5+2O10 are involved in the formation of Ca10Ir4+5Ir5+4O30. By analogy with the well-known catalyst Ca5Ir4+Ir5+2O12, the compound Ca10Ir4+5Ir5+4O30 may also be an effective catalyst in the future, for example, when producing "ecological" hydrogen from water. When using expensive metallic iridium in catalysts, it should be assumed that the homologues of the Ca20n -10Ir4+5Ir5+4O20n + 10 series may be candidates for replacing the well-known thermo- and acid-resistant catalyst Ca5Ir4+Ir5+2O12.
1. Введение
Одним из способов прогнозирования новых химических соединений (ХС) является изучение гомологических серий (ГС). Особенностью ГС считается закономерное изменение фундаментальных характеристик ХС-гомологов в пределах одной и той же ГС , . Следовательно, знание законов формирования ГС становится обязательным при поиске новых ХС различных систем химических элементов (ХЭ).
К настоящему моменту в литературе опубликованы результаты поиска ГС различных систем ХЭ. Так, известны «фазы Магнели» MnO3n – 1 (M = Mo, W) , MnO2n – 1 (M≡Ti, V) (n = 4-10) , , , WnO3n – 2 (n = 20, 38-40) и «ГС» систем (La-Ni-O) , , , и (La-Cu-O) . Однако, на наш взгляд, при отсутствии соблюдения электронейтральности формул «ГС» приведенные выше системы авторами ошибочно считаются двухкомпонентными , , , , и трехкомпонентными , , , системами ХЭ соответственно. Например, соблюдая электронейтральность формул «ГС» правильно было бы писать так:
MenO3n – 1 ≡ Me5+2Me6+n – 2O3n – 1, где (Me ≡ Mo, W) и n = 8 –12, 14;
или MenO2n – 1 , ≡ Me3+2Me4+n – 2O2n – 1, где (Me ≡ Ti, V) и n = 4-10;
или WnO3n – 2 ≡ W5+4W6+n – 4O3n – 2, где n = 20, 38-40,
а также LanNinO3n – 1 ≡ LanNi2+2Ni3+n – 2O3n – 1, Lan + 1NinO3n + 1 ≡ Lan + 1Ni2+Ni3+n –1O3n + 1, Lan + 1NinO3n – 1 ≡
≡ Lan + 1Ni2+Ni3+n –1O3n – 1и La2n – 4NinO4n – 5 ≡ La2n – 4Ni2+n – 2Ni3+2O4n – 5.
В работах и указаны причины некорректного написания авторами этих работ формул «ГС»: во-первых, формулы не являются электро нейтральными. Другой причиной этого, видимо, является отсутствие знания законов формирования ГС. Как видно, подмеченное в и изменение выше приведенных составов образцов не соответствует формулам именно ГС, а, скорее всего, является случайным сочетанием какого-то изменения состава образцов, подчиняющейся опубликованной формуле, но не формуле ГС. Так, в выше приведенных авторских формулах «ГС» могут одновременно изменяться концентрационные параметры всех двух ХЭ , , , , или всех трех ХЭ , , , , хотя, как это доказано в , в формуле именно ГС могут быть переменными концентрации только двух ХЭ, одного катиона и аниона. Другими словами, ГС могут развиваться в сторону только двухкомпонентных ХС (ДХС) .
В работах , , , , впервые представлен способ расчета формул ГС трех-, четырех- и пятикомпонентных систем ионов ХЭ. Закономерное изменение состава гомологов одной и той же ГС определяется геометрическими особенностями треугольника и треугольной пирамиды, которые представляют систему ионами ХЭ. Способ расчета основан на рассмотрении цепи последовательно протекающих химических взаимодействий компонентов системы, начиная с образования двухкомпонентных ХС-окислов. Система ионов ХЭ представляется треугольником или треугольной пирамидой, в углах основания которых помещены положительно заряженные ионы ХЭ, а в вершине помещается анион. Геометрические особенности треугольника и треугольной пирамиды позволяют проследить последовательность химических взаимодействий, в результате чего появляется возможность из всех рассматриваемых реакций выявить те, которые участвуют в формировании ГС.
Используя этот, способ рассчитаны формулы ГС систем ионов ХЭ в обобщенном виде:
AnbcBacC(n + 1)ab, AbcBnacC(n + 1)ab , A(2n – 1)bdcBadcDabcC(2n + 1)abd, AbdcBadcD(2n – 1)abcC(2n + 1)abd, AbdcB(2n – 1)adcDabcC(2n + 1)abd , ,
A{(n – 1 – k)(r + w + v) + t}bdfcBradfcDwabfc FvabdcC{(n – k)(r + w + v) + t}abdf, AtbdfcB{(n – 1 – k)(t + w + v) + r}adfcDwabfc FvabdcC{(n – k)(t + w + v) + r}abdf,
AtbdfcBradfcD{(n – 1 – k)(t + r + v) + w}abfcFvabdcC{(n – k)(t + r + v) + w}abdf, AtbdfcBradfcDwabfcF{( n – 1 – k)(t + r + w) + v}abdcC{(n – k)(t + r + w) + v}abdf , , и для конкретных систем ионов ХЭ: ( La3+ – Ni2+ – Ni3+ – O2-) , (Na+ – TI4+ – O2-), (Li+ – Ti4+ – O2–), (K+ – V5+ – O2–), (Ba2+ – ㅤ– Cu2+ – O2–){Li+ – Fe2+ – (PO4)3-} , (Zn2+ – Ge4+ – P3-) , (Li+ –Fe4+ –[Sr3La2]12+ – O2–) , (Li+ – Ni3+ – Mn3+ – O2-) , (Bi3+ – Cu2+– [SrCa]4+ – O2–) , (Li+ – Sr2+ – La3+ – Fe4+ –O2-) , (La3+ – Sr2+ – Ti4+ – O2-) , , (Bi3+ – Sr2+ – Ca2+ – ㅤ – Cu2+ – O2–) , (Ca2+ – Ir4+ – Ir5+ – O2-) , (Ir4+ – Ir5+ – O2–), (Ca2+ – Ir4+ – O2–) и (Ca2+ – Ir5+ – O2–) .
Считая «фазы Магнели» трехкомпонентными, осуществленный анализ показал, что все выше приведенные формулы «фаз Магнели» совпадают с формулами трехкомпонентных ХС (ТХС) αp-ГС при следующих условиях:
1) для MenO2n – 1 , ≡ Me3+2Me4+n – 2O2n – 1 при n = 5, 8, 11, 14 и т. д. формулы ТХС совпадают с формулами ТХС в αp-ГС Aa+bcBb+acnCc-ab(n + 1) ≡ Me3+8Me4+6nO12(n + 1) ≡ Me3+4Me4+3nO6(n + 1) при nαp = 2, 4, 6, 8 и т.д.;
2) для MenO3n – 2 ≡ Me5+4Me6+n – 4O3n – 2 при n = 14, 24, 34, 44 и т. д. формулы ТХС совпадают с формулами ТХС в αp-ГС Aa+bcBb+acnCc-ab(n + 1) ≡ Me5+6Me6+5nO15(n + 1) при nαp = 3, 6, 9, 12 и т.д.;
3) для MenO3n – 1 ≡ Me5+2Me6+n – 2O3n – 1 при n = 12, 17, 22, 27 и т. д. формулы ТХС совпадают с формулами ТХС в αp-ГС Aa+bcBb+acnCc-ab(n + 1) ≡ Me5+6Me6+5nO15(n + 1) при nαp = 6, 9, 12, 15 и т.д.
Кроме этого, например, в работе на базе пяти ЧХСn(bas) = La2Ni2+3Ni3+2O9, La4Ni2+3Ni3+6O18, La8Ni2+6Ni3+6O27, La8Ni2+6Ni3+18O45 и La4Ni2+3Ni3+12O27, рассчитано семнадцать четырехкомпонентных ГС (ЧГС). В частности, ЧГС, полученные на базе соединения La2Ni2+3Ni3+2 O9, имеют следующий вид:
La12(2n – 1)Ni2+18Ni3+12O18(2n + 1), La12Ni2+18(2n – 1)Ni3+12O18(2n + 1) и La12Ni2+18Ni3+12(2n – 1) O18(2n + 1).
Расчеты ЧГС системы (La3+ – Ni2+ – Ni3+ – O2-) в показали, что известные из работы соединения La3Ni2O7, La4Ni3O10, La5Ni4O13 и La6Ni5O16, относящихся к фазам Риддлесдена-Поппера Lan + 1NinO3n + 1 , следовало бы записать иначе с учетом того, что они относятся к четырехкомпонентным системам ХЭ. Так, расчеты в показали, что известные из работы соединения (La3Ni2O7 ≡ La6Ni2+2Ni3+2 O14 = ЧХСn = 2), (La4Ni3O10 ≡ La4Ni2+Ni3+2 O10 = ЧХСn = 2), (La5Ni4O13 ≡ La5Ni2+Ni3+3O13 = ЧХСn = 4) и (La6Ni5O16 ≡ La6Ni2+Ni3+4 O16 = = ЧХСn = 5) оказались, согласно , вторыми членами в ЧГС: La10n - 2Ni2+6Ni3+6 O15n + 12, La8n - 4Ni2+3Ni3+6 O12n + 6, La22n - 14Ni2+6Ni3+18 O33n + 12 и La14n - 10Ni2+3Ni3+12 O21n + 6. В ЧХС рассчитывались на базе ЧХСn(bas) = La8Ni2+6Ni3+6O27, La4Ni2+3 Ni3+6 O18, La8Ni2+6Ni3+18O45 и La4Ni2+3Ni3+12O27, соответственно. Как видно, формулы из работы принципиально отличаются от опубликованных в работах , , и формул.
Важно отметить, что рассчитанные в работе формулы трехкомпонентных ГС (ТГС) системы (M+ – Ti4+ – O2-), где M+ ≡ Li+, Na+, K+, полностью совпадают с формулой ТГС, полученной только на основе экспериментов , что говорит о работоспособности разработанного в , , , способа расчета ГС многокомпонентных систем ионов ХЭ.
Расчет ГС систем (Ca2+ – Ir4+ – Ir5+ – O2-) и подсистем (Ir4+ – Ir5+ – O2–), (Ca2+ – Ir4+ –O2–) и (Ca2+ – Ir5+ – O2–) с участием разно валентного иридия представляет интерес при поиске новых составов ХС, используемых в качестве электролитических катализаторов для производства «экологического» водорода путем электролитического разложения воды и для анодной реакции выделения кислорода в сильно кислотном электролите . Поиск новых иридий содержащих катализаторов актуален из-за высокой стоимости и дефицита металлического иридия . Это возможно, если эти исследования будут способствовать повышению каталитической активности нового состава образцов с участием разно валентного иридия, Ir4+ и Ir5+. Так, в работе для системы (Ca2+ – Ir4+ – Ir5+ – O2-) на базе соединения Ca5Ir4+Ir5+2O12, содержащего Ir4+ и Ir5+ в соотношении 1/2 , , рассчитаны формулы трех ГС, которые развиваются в сторону CaO, IrO2 и Ir2O5: Ca7n – 2Ir4+Ir5+2O7n + 5, Ca5Ir4+Ir5+5n - 4O10n + 2 и Ca25Ir4+5Ir5+14n - 4O35n + 25. Расчетами ГС трехкомпонентных подсистем (Ir4+ – Ir5+ – O2–), (Ca2+ – Ir5+ –O2–) и (Ca2+ – Ir4+ – O2–) на базе соединений Ir4+5Ir5+4O20, Ca5Ir5+2O10, и Ca2Ir4+O4, соответственно, получены следующие формулы ГС: Ir4+5Ir5+4nO10n + 10, Ir4+5nIr5+4O10n + 10, Ca5Ir5+2nO5n + 5, Ca5nIr5+2O5n + 5, Ca2Ir4+nO2n + 2 и Ca2nIr4+O2n + 2, соответственно. Причем, для подсистемы (Ca2+ – Ir4+ – O2–) известные из экспериментальных работ , , , и соединения (Ca2Ir4+O4 = ТХСn(bas) = 1) и (Ca2Ir4+2O6 = ТХСn = 2) принадлежат αm-ГС, Ca2Ir4+nO2n + 2, которые развиваются в сторону IrO2, а соединения (Ca2Ir4+O4 = ТХСn(bas) = 1) и (Ca4Ir4+O6 = ТХСn = 2), принадлежат αp-ГС, Ca2nIr4+O2n + 2, которые развиваются в сторону CaO. Сказанное, также как расчеты ГС системы ((M+-Ti4+-O2-) , говорит о работоспособности разработанного в работах , , , способа расчета формул ГС многокомпонентных систем ионов ХЭ.
Цель работы: в настоящей работе продолжены расчеты четырехкомпонентных ГС ХС (ЧГС) системы (Ca2+ – ㅤ – Ir4+ – Ir5+ – O2-) на базе соединения Ca5Ir4+Ir5+2O12 расчетами ЧГС на базе соединения Ca10Ir4+5Ir5+4O30 с использованием полученных расчетом в работе трехкомпонентных ТХС, (Ca2Ir4+O4 = ТХСn(bas) = 1), (Ca5Ir5+2O10 = ТХСn(bas) = 1) и (Ir4+5Ir5+4O20 = ТХСn(bas) = 1).
2. Основная часть
2.1. Система (Ca2+ – Ir4+ – Ir5+ – O2-)
В настоящей работе при расчете ЧГС системы (Ca2+ – Ir4+ – Ir5+ – O2-) кластер Ca10Ir4+5Ir5+4O30 является базовым, (ЧХСn(bas) = 1 = т. 10 = Ca10Ir4+5Ir5+4O30). При представлении системы ионов ХЭ треугольником или треугольной пирамидой химические реагенты и продукты их взаимодействия в виде ХС или заряженного кластера (ЗК) располагаются на одном и том же отрезке прямой , . Согласно работам , любые ХС и ЗК находятся в точке пересечения отрезков, представляющих несколько разных пар реагентов. Следовательно, одной из реакций образования кластера Ca10Ir4+5Ir5+4O30 является взаимодействие ТХСn(bas) = 1 в виде т. 2, т. 5 и т. 8 с CaO, IrO2 и Ir2O5, соответственно, что отображается на рис. 1 пересечением отрезков (т. 2 – CaO), (т. 5 – IrO2) и (т. 8 – Ir2O5) в т. 10, где ㅤ(т. 10 = ЧХСn(bas) = 1 = Ca20Ir4+10Ir5+8O60) на рис. 1:
Кластеры в виде т. 2, т. 5 и т. 8 принадлежат подсистемам (Ir4+ – Ir5+ – O2–), (Ca2+ – Ir5+ – O2–) и (Ca2+ – Ir4+ – O2–), соответственно. Cогласно , эти кластеры в виде т. 2, т. 5 и т. 8 также могут быть получены в результате окисления двухкомпонентных ХС (ДЗКn(bas) = 1) в виде (т. 3 = [Ir4+5Ir5+4]40+ = ДЗКn(bas) = 1), (т. 6 = [Ca5Ir5+2]20+ = = ДЗКn(bas) = 1) и (т. 9 = [Ca2Ir4+]8+ = ДЗКn(bas) = 1), соответственно.
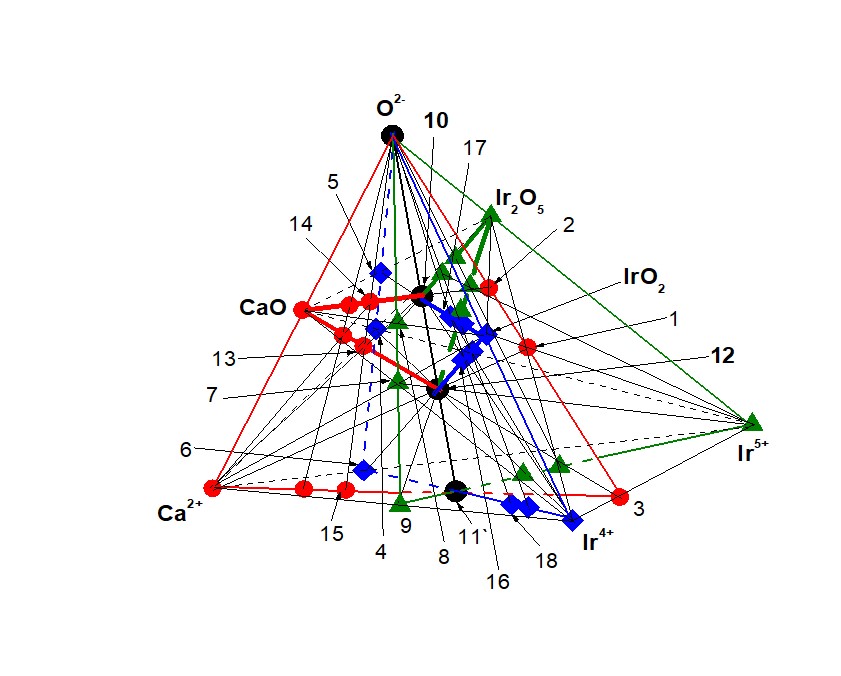
Рисунок 1 - Система (Ca2+ – Ir4+ – Ir5+ – O2-) на базе соединения Ca10Ir4+5Ir5+4O30
т. 3 = ДЗКn(bas) = 1 = [Ir4+5Ir5+4]40+, т. 4 = ТЗКn(bas) = 1 = [Ca5Ir5+2O5]10+,
т. 5 = ТХСn(bas) = 1 = Ca5Ir5+2O10, т. 6 = ДЗКn(bas) = 1 = [Ca5Ir5+2]20+,
т. 7 = ТЗКn(bas) = 1 = [Ca2Ir4+O2]4+, т. 8 = ТХСn(bas) = 1 = Ca2Ir4+O4,
т. 9 = ДЗКn(bas) = 1 = [Ca2Ir4+]8+, т. 10 = ЧХСn(bas) = 1 = Ca10Ir4+5Ir5+4O30,
т. 11 = ТЗКn(bas) = 1 = [Ca10Ir4+5 Ir5+4]60+, т. 12 = ЧХСn(bas) = 1 = [Ca10Ir4+5Ir5+4O10]40+,
т. 13 = ЧХСn = 2 = [Ca30Ir4+5 Ir5+4O30]40+, т. 14 = ЧЗКn = 2 = Ca30Ir4+5 Ir5+4O50,
т. 15 = [Ca30Ir4+5 Ir5+4]100+, т. 16 = ЧЗКn = 2 = [Ca10Ir4+15Ir5+4O30]40+,
т. 17 = ЧХСn = 2 = Ca10Ir4+15Ir5+4O50, т. 18 = [Ca10Ir4+15Ir5+4]100+
Кластер ([Ca10Ir4+5Ir5+4O10]40+ = ЧЗКn(bas) = 1 = т. 12), также являющийся базовым, образуется не только в результате взаимодействия кластеров в виде т. 3, т. 6 и т. 9 с CaO, IrO2 и Ir2O5, но и при взаимодействии кластеров в виде т 1, т. 4 и т.7 с Ca2+, Ir4+ b Ir5+, соответственно (рис.1):
В свою очередь, согласно работе , кластеры в виде т. 1, т. 4 и т. 7 образуются так:
Именно кластеры в виде т. 1, т. 4 и т. 7, образующиеся по реакциям (3), (4) и (5), обусловливают пересечение отрезков (т. 1 – Ca2+), (т. 4 – Ir4+) b (т. 7 – Ir5+) в одной точке в виде кластера ([Ca10Ir4+5Ir5+4O10]40+ = т. 12 = ЧЗКn(bas) = 1). Сказанное описывается уравнением (2) на рис. 1. Базовый кластер (ЧЗКn(bas) = 1 = т. 10 = Ca10Ir4+5Ir5+4O30) образуется не только по реакции (1), но и при окислении кластеров в виде т. 12 и т. 11– рис. 1:
Кластер ([Ca10Ir4+5 Ir5+4]60+ = ТЗКn(bas) = 1 = т. 11), также участвовавший в образовании базового кластера (Ca10Ir4+5Ir5+4O30 = ЧХСn(bas) = 1 = т. 10), согласно реакции (6), образуется в результате взаимодействия кластеров в виде т. 3, т. 6 и т. 9 с Ca2+, Ir4+ и Ir5+, соответственно:
Согласно работе , ГС могут развиваться только в сторону двухкомпонентных ХС-окислов CaO, IrO2 и Ir2O5, что и будет учитываться ниже.
2.1.1. Подсистема (Ca2+ – т. 3 – O2-). Направление CaO
Четырехкомпонентная ГС-1, которая развивается в сторону CaO, формируется в подсистеме (т. 3 – Ca2+ – O2-) на рис. 1, 2. Согласно , , и рис. 1, 2, базовый кластер (Ca10Ir4+5Ir5+4O30= ЧХСn(bas) = 1 = т. 10) может взаимодействовать только с Ca2+, образуя кластер в виде (т. 13 = ЧЗКn(bas) + 1 = 2), чем и начинает формировать ГС-1. Кластер в виде т. 13 также может быть получен взаимодействием кластера в виде т. 3 с CaO, о чем свидетельствует пересечение соответствующих отрезков прямых (т. 10 – Ca2+) и (т. 3 – CaO) на рис.1, 2:
В свою очередь, окисление кластера в виде т. 13 и взаимодействие кластера в виде т. 2 с CaO приводит к образованию в ГС-1 второго гомолога в виде (т. 14 = ЧХСn(bas) + 1 = 2):
Тогда гомологическая разница Δ определится так:
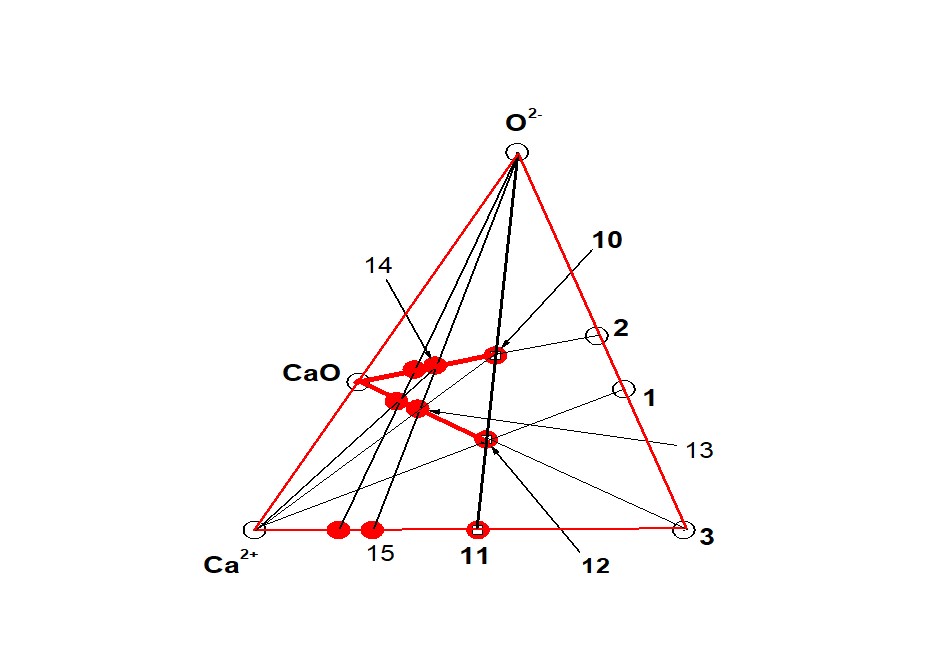
Рисунок 2 - Подсистема (Ca2+ – т. 5 – O2–). Направление CaO
т. 3 = ДЗКn(bas) = 1 = [Ir4+5Ir5+4]40+, т. 10 = ЧХСn(bas) = 1 = Ca10Ir4+5Ir5+4O30,
т. 11 = ТЗКn(bas) = 1 = [Ca10Ir4+5 Ir5+4]60+, т. 12 = ЧХСn(bas) = 1 = [Ca10Ir4+5Ir5+4O10]40+,
т. 13 = ЧЗКn(bas) + 1 = 2 = [Ca30Ir4+5 Ir5+4O30]40+,
т. 14 = ЧХСn(bas) + 1 = 2 = Ca30Ir4+5 Ir5+4O50, т. 15 = [Ca30Ir4+5 Ir5+4]100+
Так как (ТХСn = ТХСn = 1 + k∙Δ), (ТХСn = 1 = ТХСn(bas) – kbas∙Δ) и (n(bas) = kbas + 1), то выясняется, что при определении ТХСn = 1, вычитать формулу (Δ = Ca20O20) из формулы (Ca10Ir4+5Ir5+4O30= = ЧХСn(bas) = 1 = т. 10) нельзя. Следовательно, kbas = 0 и n(bas) = 1. Тогда получим:
2.1.2. Подсистема (Ir4+ – т. 6 – O2-). Направление IrO2
Четырехкомпонентная ГС-2, которая развивается в сторону IrO2, формируется в подсистеме (т. 6 – Ir4+ – O2-) на рис. 1, 3. Базовым кластером для ГС-2 также является кластер (Ca10Ir4+5Ir5+4O30= ЧХСn(bas) = 1 = т. 10 ). Формирование ГС-2 идет по той же схеме, что и формирование ГС-1: кластер (Ca10Ir4+5Ir5+4O30= ЧХСn(bas) = 1 = т. 10) может взаимодействовать только с Ir4+ , , . Пересечение отрезков (т. 10 – Ir4+) и (т. 6 – IrO2) отражает образование в ГС-2 кластера в виде (т. 16 =ЧЗКn(bas) + 1 = 2), а пересечение отрезков (т.16 – O2-) и (т. 5 – IrO2) в т.17 соответствуют образованию в ГС-2 второго гомолога в виде (т. 17 = ЧХСn(bas) + 1 = 2), что описывается следующими уравнениями реакций на рис. 1, 3:
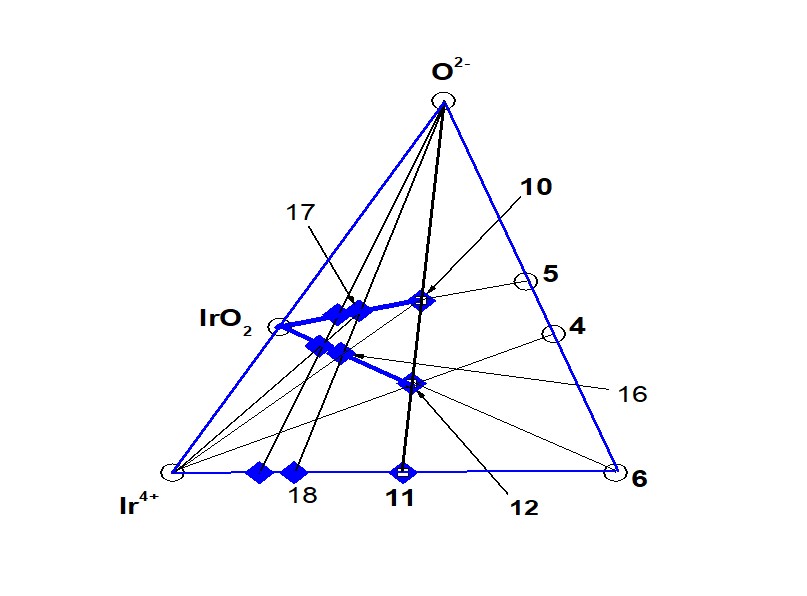
Рисунок 3 - Подсистема (Ir4+ – т. 6 – O2–). Направление IrO2
т. 6 = ДЗКn(bas) = 1 = [Ca5Ir5+2]20+, т. 10 = ЧХСn(bas) = Ca10Ir4+5Ir5+4O30,
т. 11 = ТЗКn(bas) = 1 = [Ca10Ir4+5 Ir5+4]60+, т. 12 = ЧХСn(bas) = [Ca10Ir4+5Ir5+4O10]40+,
т. 16 = ЧЗКn(bas) + 1 = 2 = [Ca10Ir4+15Ir5+4O30]40+,
т. 17 = ЧХСn(bas) + 1 = 2 = Ca10Ir4+15Ir5+4O50, т. 18 = [Ca10Ir4+15Ir5+4]100+
Гомологическая разница Δ определится так:
Так как (ТХСn = ТХСn = 1 + k∙Δ), (ТХСn = 1 = ТХСn(bas) – kbas∙Δ) и (n(bas) = kbas + 1), то выясняется, что при определении ТХСn = 1, вычитать формулу (Δ = Ir4+10O20) из формулы (Ca10Ir4+5Ir5+4O30 = ТХСn(bas) = 1 = т. 10 ) нельзя. Следовательно, kbas = 0 и n(bas) = 1. Тогда получим:
2.1.3. Подсистема (Ir5+ – т. 9 – O2-). Направление Ir2O5
Гомологическая серия ГС-3, которая развивается в сторону Ir2O5, формируется в подсистеме (т. 9 – Ir5+ – O2-) на рис. 1, 4. Базовым кластером для ГС-3 также является кластер (Ca10Ir4+5Ir5+4O30= ЧХСn(bas) = 1 = т. 10). Формирование ГС-3 идет по той же схеме, что и формирование ГС-1 и ГС-2: базовый кластер (Ca10Ir4+5Ir5+4O30 = ЧХСn(bas) = 1 = т. 10) может взаимодействовать только с Ir5+ , , . Пересечение отрезков (т. 10 – Ir5+) и (т. 9 – Ir2O5) отражает образование в ГС-3 второго гомолога в виде (т. 19 = ЧЗКn(bas) + 1 = 2), а пересечение отрезков (т. 19 – O2-) и (т. 8 – Ir2O5) в т. 20 соответствуют образованию в ГС-3 второго гомолога в виде (т. 20 = ЧХСn(bas) + 1 = 2), что описывается следующими уравнениями реакций на рис. 1, 4:
Гомологическая разница Δ определится так:
Так как (ТХСn = ТХСn = 1 + k∙Δ), (ТХСn = 1 = ТХСn(bas) – kbas∙Δ) и (n(bas) = kbas + 1), то выясняется, что при определении ТХСn = 1, вычитать формулу (Δ = Ir5+14O35) из формулы (Ca10Ir4+5Ir5+4O30 = ТХСn(bas) = 1 = т. 10 ) нельзя. Следовательно, kbas = 0 и n(bas) = 1. Тогда получим:
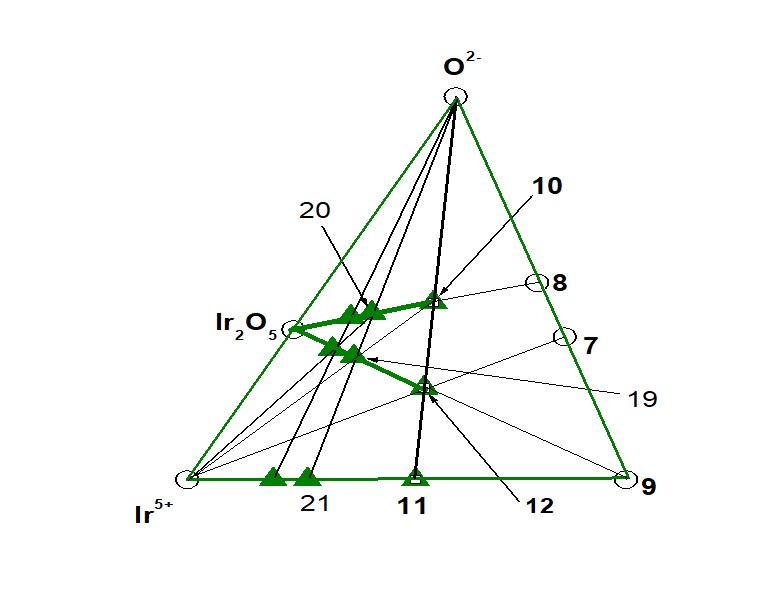
Рисунок 4 - Подсистема (Ir5+ – т. 7 – O2–). Направление Ir2O5
т. 9 = ДЗКn(bas) = 1 = [Ca2Ir4+]8+,т. 10 = ЧХСn(bas) = 1 = Ca10Ir4+5Ir5+4O30,
т. 11 = [Ca10Ir4+5 Ir5+4]60+, т. 12 = ЧХСn(bas) = 1 = [Ca10Ir4+5Ir5+4O10]40+,
т. 19 = ЧЗКn(bas) + 1 = 2 = [Ca10Ir4+5 Ir5+12O30]40+,
т. 20 = ЧХСn(bas) + 1 = 2 = Ca10Ir4+5 Ir5+12O50, т. 21 = [Ca10Ir4+5 Ir5+12]100+
На рис. 5 для сравнения представлены гомологические серии, сформированные в подсистеме (CaO – IrO2 – Ir2O5) на базе соединений Ca5Ir4+Ir5+2O12 и Ca10Ir4+5Ir5+4O30. При условии, что существование (ЧХСn = 3 = т. 30 = Ca5Ir4+11Ir5+2O32) и (ЧХСn = 3 = т. 23 = Ca10Ir4+25Ir5+4O70) – членов ГС, сформированных на базе (ЧХСn(bas) = 1 = т. 25 = Ca5Ir4+Ir5+2O12) и (ЧХСn(bas) = 1 = т. 10 = Ca10Ir4+5Ir5+4O30), будет подтверждено экспериментально, интересно сравнить свойства кластеров в виде т. 30 и т. 23. Так, если допустить существование влияния на процесс катализа окислительно-восстановительной реакции (Ir4+ ↔ Ir5+ + ē ), то близко расположенные составы ЧХС в виде т. 30 и т. 23, обладающие различным соотношением Ir4+/Ir5+ = 11/2 = 5,5 и Ir4+/Ir5+ = 25/4 = 6,25, соответственно, вероятнее всего, могут представлять интерес с точки зрения изучения влияния соотношения Ir4+/Ir5+ на эффективность катализа из-за различных условий наступления динамического равновесия в этом процессе.
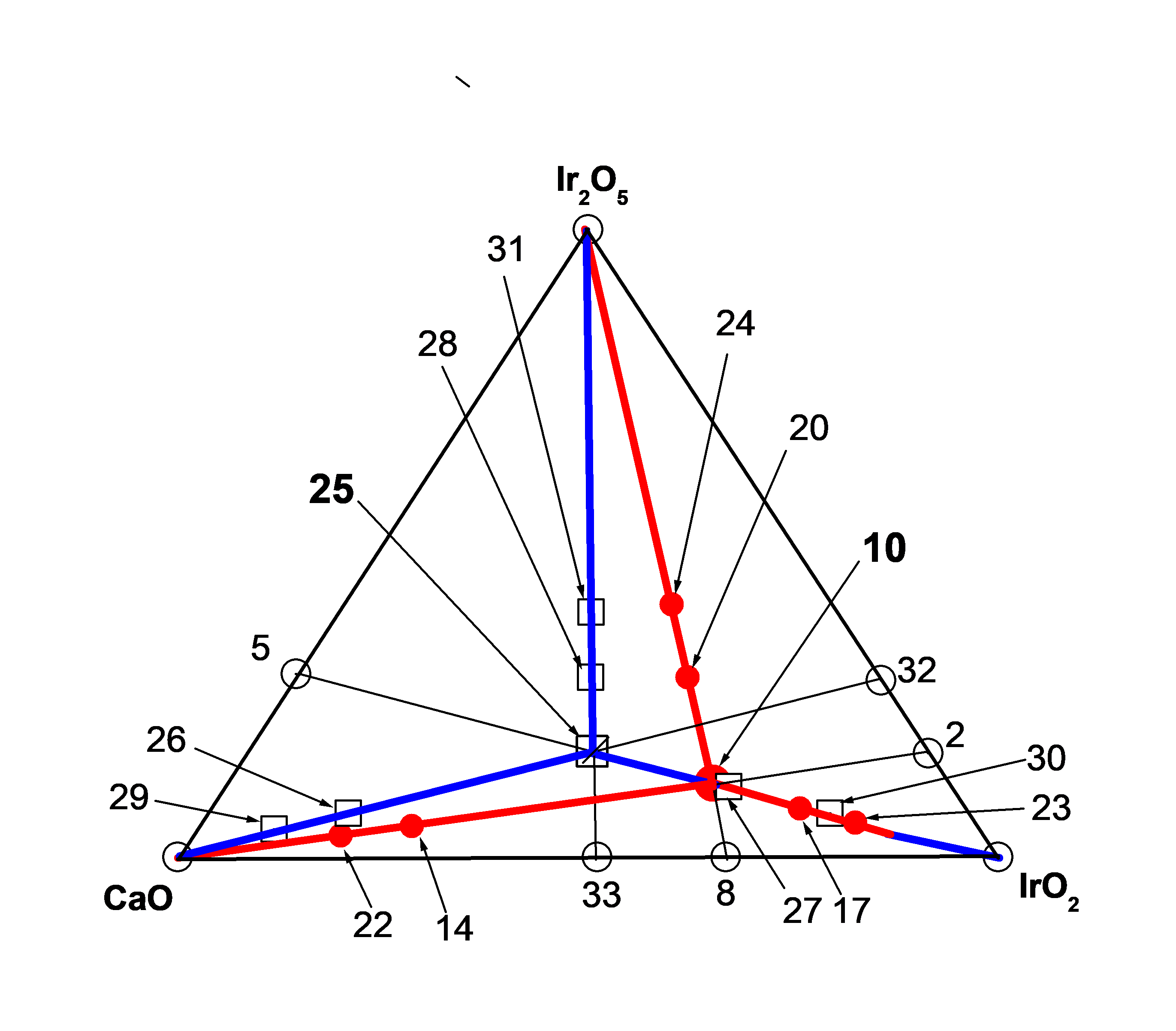
Рисунок 5 - Подсистема (CaO – IrO2 – Ir2O5)
Кроме этого, важно сравнить влияние на каталитические свойства кристаллической структуры ХС (Ca5Ir4+11Ir5+2O32 = т. 30 =ЧХСn = 3) и (Ca10Ir4+25Ir5+4O70 = т. 23 = ЧХСn = 3), расположенных на одном и том же отрезке (т. 5 – IrO2), но гомологически связанных с разными базовыми ЧХСn(bas) = 1 = Ca5Ir4+Ir5+2O12 и Ca10Ir4+5Ir5+4O30 — основателями разных ЧГС.
3. Заключение
Расчет ГС ХС системы (Ca2+ – Ir4+ – Ir5+ – O2-) осуществлен при представлении системы ионами ХЭ и рассмотрением цепи последовательно протекающих химических взаимодействий компонент системы начиная с образования CaO, IrO2 и Ir2O5. Геометрические особенности треугольной пирамиды, представляющей систему ионов ХЭ, позволили из всех рассмотренных реакций химического взаимодействия выбрать те, которые отвечают за формирование ГС. При расчете использован базовый кластер (Ca10Ir4+5Ir5+4O30 = = ЧХСn(bas) = 1), одной из реакций образования которого является взаимодействие первых гомологов ТХСn(bas) = 1 трехкомпонентных подсистем (Ir4+ – Ir5+ – O2-), (Ca2+ – Ir4+ – O2-) и (Ca2+ – Ir5+ – O2-): Ir4+5Ir5+4O20, Ca2Ir4+O4, и Ca5Ir5+2O10.
Рассчитанные формулы ЧГС развиваются в сторону CaO, IrO2 и Ir2O5 и имеют следующий вид: Ca20n -10Ir4+5Ir5+4O20n + 10, Ca10Ir4+10n - 5Ir5+4O20n + 10 и Ca10Ir4+5Ir5+8n - 4O20n + 10. Графическое представление ЧГС, сформированных в подсистеме (CaO – IrO2 – Ir2O5) на базе соединений Ca5Ir4+Ir5+2O12 и Ca10Ir4+5Ir5+4O30, дают повод для изучения возможного влияния процесса окисление-восстановление (Ir4+ ↔ Ir5+ + ē) на процесс катализа. Полученные формулы ЧГС дают возможность везти поиск новых соединений – возможно, лучших претендентов на замену уже известных, используемых в качестве катализаторов при получении «экологического» водорода.
